(DOU de 02.04.2026)
Altera a Instrução Normativa n° 28, de 26 de julho de 2018, que estabelece as listas de constituintes, de limites de uso, de alegações e de rotulagem complementar dos suplementos alimentares.
A DIRETORIA COLEGIADA DA AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA, no uso da atribuição que lhe confere o art. 15, III e IV, aliado ao art. 7°, III da Lei n° 9.782, de 26 de janeiro de 1999, e ao art. 187, VII, § 1° do Regimento Interno aprovado pela Resolução da Diretoria Colegiada – RDC n° 585, de 10 de dezembro de 2021, resolve adotar a seguinte Instrução Normativa, conforme deliberado em reunião realizada em 1° de abril de 2026, e eu, Diretor-Presidente, determino a sua publicação.
Art. 1° Esta Instrução Normativa altera a Instrução Normativa – IN n° 28, de 26 de julho de 2018, publicada no Diário Oficial da União n° 144, de 27 de julho de 2018, Seção 1, pág.141, que estabelece as listas de constituintes, de limites de uso, de alegações e de rotulagem complementar dos suplementos alimentares, para atualizar a:
I – “Lista de constituintes autorizados para uso em suplementos alimentares, exceto para os suplementos alimentares indicados para lactentes (0 a 12 meses) ou crianças de primeira infância (1 a 3 anos)”, disposta em seu Anexo I;
II – “Lista de limites mínimos de nutrientes, substâncias bioativas, enzimas e probióticos que devem ser fornecidos pelos suplementos alimentares, na recomendação diária de consumo e por grupo populacional indicado pelo fabricante”, disposta em seu Anexo III;
III – “Lista dos limites máximos de nutrientes, substâncias bioativas, enzimas e probióticos que não podem ser ultrapassados pelos suplementos alimentares, na recomendação diária de consumo e por grupo populacional indicado pelo fabricante”, disposta em seu Anexo IV;
IV – “Lista de alegações autorizadas para uso na rotulagem dos suplementos alimentares e os respectivos requisitos de composição e de rotulagem”, disposta em seu Anexo V; e
V – “Lista de requisitos de rotulagem complementar dos suplementos alimentares”, disposta em seu Anexo VI.
Art. 2° A “Lista de constituintes autorizados para uso em suplementos alimentares, exceto para os suplementos alimentares indicados para lactentes (0 a 12 meses) ou crianças de primeira infância (1 a 3 anos) do Anexo I da Instrução Normativa – IN n° 28, de 26 de julho de 2018, passa a vigorar com o acréscimo dos constituintes relacionados no Anexo I desta Instrução Normativa.
Art. 3° A “Lista de limites mínimos de nutrientes, substâncias bioativas, enzimas e probióticos que devem ser fornecidos pelos suplementos alimentares na recomendação diária de consumo e por grupo populacional indicado pelo fabricante” do Anexo III da Instrução Normativa – IN n° 28, de 26 de julho de 2018, passa a vigorar com o acréscimo dos limites relacionados no Anexo II desta Instrução Normativa.
Art. 4° A “Lista de limites máximos de nutrientes, substâncias bioativas, enzimas e probióticos que não podem ser ultrapassados pelos suplementos alimentares na recomendação diária de consumo e por grupo populacional indicado pelo fabricante” do Anexo IV da Instrução Normativa – IN n° 28, de 26 de julho de 2018, passa a vigorar com o acréscimo dos limites relacionados no Anexo III desta Instrução Normativa.
Art. 5° A “Lista de alegações autorizadas para uso na rotulagem dos suplementos alimentares e os respectivos requisitos de composição e de rotulagem”, do Anexo V da Instrução Normativa – IN n° 28, de 26 de julho de 2018, passa a vigorar com o acréscimo das alegações relacionadas no Anexo IV desta Instrução Normativa.
Art. 6° A “Lista de requisitos de rotulagem complementar dos suplementos alimentares” do Anexo VI da Instrução Normativa – IN n° 28, de 26 de julho de 2018, passa a vigorar com o acréscimo dos requisitos de rotulagem complementar relacionados no Anexo V desta Instrução Normativa.
Art. 7° Esta Instrução Normativa entra em vigor na data de sua publicação.
LEANDRO PINHEIRO SAFATLE
Diretor-Presidente
ANEXO I
CONSTITUINTES INCLUÍDOS NA “LISTA DE CONSTITUINTES AUTORIZADOS PARA USO EM SUPLEMENTOS ALIMENTARES, EXCETO PARA OS SUPLEMENTOS ALIMENTARES INDICADOS PARA LACTENTES (0 A 12 MESES) OU CRIANÇAS DE PRIMEIRA INFÂNCIA (1 A 3 ANOS)” DO ANEXO I DA INSTRUÇÃO NORMATIVA – IN N° 28, DE 26 DE JULHO DE 2018.
| NUTRIENTES | |
| Lipídeos | CAS |
| Óleo de amêndoa de baru | – |
| Óleo de microalgas Schizochytrium sp. ATCC PTA-9695 com DHA | – |
| SUBSTÂNCIAS BIOATIVAS | |
| Polifenóis do açaí | CAS |
| Concentrado de açaí liofilizado | – |
| Antocianinas do açaí | CAS |
| Concentrado de açaí liofilizado | – |
| PROBIÓTICOS | CAS |
| Bifidobacterium animalissubsp.lactisCCT 7858 | – |
| Streptococcus salivariusK12 | CAS |
| Associação deBifidobacterium animalissubsp.lactisHN019 (ATCC SD5674),Lactobacillus acidophilusNCFM (ATCC SD5221),Lactobacillus rhamnosusHN001 (ATCC SD5675),Lactobacillus paracasei Lpc-37 (ATCC SD5275) e Fruto-oligossacarídeos (FOS) | – |
ANEXO II
LIMITES MÍNIMOS INCLUÍDOS NA “LISTA DE LIMITES MÍNIMOS DE NUTRIENTES, SUBSTÂNCIAS BIOATIVAS, ENZIMAS E PROBIÓTICOS QUE DEVEM SER FORNECIDOS PELOS SUPLEMENTOS ALIMENTARES NA RECOMENDAÇÃO DIÁRIA DE CONSUMO E POR GRUPO POPULACIONAL INDICADO PELO FABRICANTE” DO ANEXO III DA INSTRUÇÃO NORMATIVA – IN N° 28, 26 DE JULHO DE 2018.
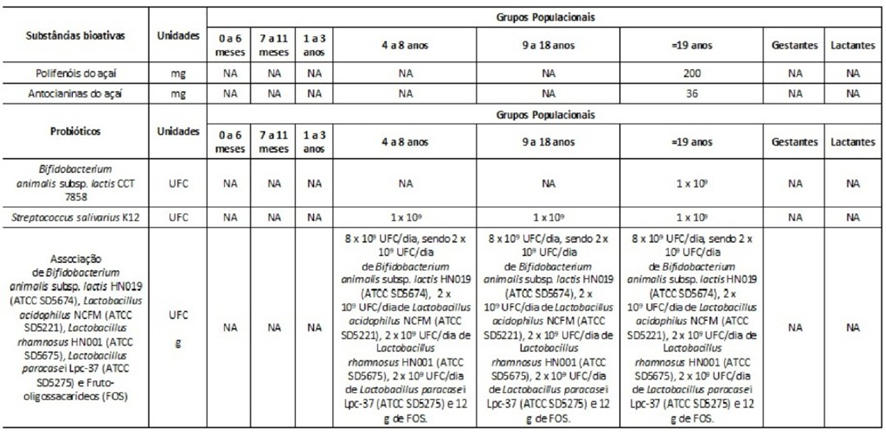
ANEXO III
LIMITES MÁXIMOS INCLUÍDOS OU ALTERADOS NA “LISTA DOS LIMITES MÁXIMOS DE NUTRIENTES, SUBSTÂNCIAS BIOATIVAS, ENZIMAS E PROBIÓTICOS QUE NÃO PODEM SER ULTRAPASSADOS PELOS SUPLEMENTOS ALIMENTARES NA RECOMENDAÇÃO DIÁRIA DE CONSUMO E POR GRUPO POPULACIONAL INDICADO PELO FABRICANTE” DO ANEXO IV DA INSTRUÇÃO NORMATIVA – IN N° 28, DE 26 DE JULHO DE 2018.
| Substâncias bioativas | Unidades | Grupos Populacionais | |||||||
| 0 a 6 meses | 7 a 11 meses | 1 a 3 anos | 4 a 8 anos | 9 a 18 anos | ≥ 19 anos | Gestantes | Lactantes | ||
| Polifenóis do açaí | mg | NA | NA | NA | NA | NA | 825 | NA | NA |
| Antocianinas do açaí | mg | NA | NA | NA | NA | NA | 150 | NA | NA |
| Probióticos | Unidades | Grupos Populacionais | |||||||
| 0 a 6 meses | 7 a 11 meses | 1 a 3 anos | 4 a 8 anos | 9 a 18 anos | ≥ 19 anos | Gestantes | Lactantes | ||
| Bifidobacterium animalissubsp.lactisCCT 7858 | UFC | NA | NA | NA | NA | NA | NE | NA | NA |
| Streptococcus salivariusK12 | UFC | NA | NA | NA | NE | NE | NE | NA | NA |
| Associação deBifidobacterium animalissubsp.lactisHN019 (ATCC SD5674),Lactobacillus acidophilusNCFM (ATCC SD5221),Lactobacillus rhamnosusHN001 (ATCC SD5675),Lactobacillus paracasei Lpc-37 (ATCC SD5275) e Fruto-oligossacarídeos (FOS) | UFC g | NA | NA | NA | NE | NE | NE | NA | NA |
ANEXO IV
ALEGAÇÕES INCLUÍDAS NA “LISTA DE ALEGAÇÕES AUTORIZADAS PARA USO NA ROTULAGEM DOS SUPLEMENTOS ALIMENTARES E RESPECTIVOS REQUISITOS DE COMPOSIÇÃO E DE ROTULAGEM” DO ANEXO V DA INSTRUÇÃO NORMATIVA – IN N° 28, DE 26 DE JULHO DE 2018.
| Constituintes | Alegações autorizadas | Requisitos específicos de composição e rotulagem |
| Tiamina | A tiamina auxilia na função normal do sistema nervoso. | A alegação é restrita aos suplementos alimentares cuja quantidade de tiamina atenda aos valores mínimos estabelecidos no Anexo III desta Instrução Normativa. O termo “vitamina B1” pode ser usado em substituição ao termo “tiamina” nas alegações. |
| Vitamina B12 | A vitamina B12 auxilia na função normal do sistema nervoso. | As alegações são restritas aos suplementos alimentares cuja quantidade de vitamina B12 atenda aos valores mínimos estabelecidos no Anexo III desta Instrução Normativa. O termo “cianocobalamina” pode ser usado em substituição ao termo “vitamina B12” nas alegações. |
| Vitamina B6 | A vitamina B6 auxilia na função normal do sistema nervoso. | As alegações são restritas aos suplementos alimentares cuja quantidade de vitamina B6 atenda aos valores mínimos estabelecidos no Anexo III desta Instrução Normativa. O termo “piridoxina” pode ser usado em substituição ao termo “vitamina B6” nas alegações. |
| Bifidobacterium animalissubsp.lactisCCT 7858 | OBifidobacterium animalissubsp.lactisCCT 7858 pode contribuir com a saúde do trato gastro intestinal. | A alegação é restrita aos suplementos alimentares cuja quantidade mínima deBifidobacterium animalissubsp.lactisCCT 7858 fornecida na recomendação diária de consumo do produto atenda aos valores mínimos estabelecidos no Anexo III desta Instrução Normativa. |
| Streptococcus salivariusK12 | OStreptococcus salivariusK12 pode reduzir o risco de infecções das vias aéreas superiores de crianças com idade superior a três anos e adultos. | A alegação é restrita aos suplementos alimentares cuja quantidade mínima deStreptococcus salivariusK12 fornecida na recomendação diária de consumo do produto atenda aos valores mínimos estabelecidos no Anexo III desta Instrução Normativa. |
| Associação deBifidobacterium animalissubsp.lactisHN019 (ATCC SD5674),Lactobacillus acidophilusNCFM (ATCC SD5221),Lactobacillus rhamnosusHN001 (ATCC SD5675),Lactobacillus paracasei Lpc-37 (ATCC SD5275) e Fruto-oligossacarídeos (FOS) | A associação deBifidobacterium animalissubsp.lactisHN019 (ATCC SD5674),Lactobacillus acidophilusNCFM (ATCC SD5221),Lactobacillus rhamnosusHN001 (ATCC SD5675),Lactobacillus paracasei Lpc-37 (ATCC SD5275) e Fruto-oligossacarídeos (FOS) pode contribuir com a saúde do trato gastrointestinal. | A alegação é restrita aos suplementos alimentares cuja quantidade mínima deBifidobacterium animalissubsp.lactisHN019 (ATCC SD5674),Lactobacillus acidophilusNCFM (ATCC SD5221),Lactobacillus rhamnosusHN001 (ATCC |
| SD5675),Lactobacillus paracasei Lpc-37 (ATCC SD5275) e Fruto-oligossacarídeos (FOS) fornecida na recomendação diária de consumo do produto atenda aos valores mínimos estabelecidos no Anexo III desta Instrução Normativa. |
ANEXO V
REQUISITOS DE ROTULAGEM COMPLEMENTAR INCLUÍDOS NA “LISTA DOS REQUISITOS DE ROTULAGEM COMPLEMENTAR DOS SUPLEMENTOS ALIMENTARES” DO ANEXO VI DA INSTRUÇÃO NORMATIVA – IN N° 28, DE 26 DE JULHO DE 2018.
| Concentrado de açaí liofilizado | A advertência “Este produto não deve ser consumido por gestantes, lactantes e crianças.” deve constar na rotulagem do produto. |
| Bifidobacterium animalissubsp.lactisCCT 7858 | A advertência “Este produto não deve ser consumido por gestantes, lactantes, lactentes, crianças, pessoas imunocomprometidas ou pessoas acometidas de condição de saúde debilitante grave.” deve constar na rotulagem do produto. |
| Streptococcus salivariusK12 Bifidobacterium animalissubsp.lactisHN019 (ATCC SD5674),Lactobacillus acidophilusNCFM (ATCC SD5221),Lactobacillus rhamnosusHN001 (ATCC SD5675),Lactobacillus paracasei Lpc-37 (ATCC SD5275) e Fruto-oligossacarídeos (FOS) | A advertência “Este produto não deve ser consumido por gestantes, lactantes, lactentes, crianças de até 3 anos de idade, pessoas imunocomprometidas ou pessoas acometidas de condição de saúde debilitante grave.” deve constar na rotulagem do produto. |
